Imagen: Ester Inbar, Wikimedia Commons
El escorpión palestino amarillo (Leiurus quinquestriatus) es una pequeña criatura de entre 9 y 11 cm de longitud que vive en los desiertos de Oriente Medio. Durante los últimos millones de años este animal se ha especializado en capturar pequeñas presas a las que clava su aguijón. En pocos segundos, el veneno alcanza el cerebro de la víctima y la deja paralizada gracias, entre otras sustancias, a una molécula llamada clorotoxina que bloquea los canales iónicos de cloruro e interrumpe el metabolismo celular.
Este pequeño péptido fue identificado en el año 1993 por un equipo de investigadores de Harvard, que desentrañaron el mecanismo por el que el veneno del escorpión paraliza los músculos de sus presas. La pequeña cadena de 36 aminoácidos bloquea los canales que las células utilizan para pasar el cloruro a través de sus membranas, de modo que le impide avanzar. Un año después, una estudiante de doctorado de la Universidad de Alabama llamada Nicole Ullrich estaba investigando uno de los tipos de cáncer más letales, el glioma, y buscaba una forma de impedir que las células tumorales se desplazaran. La mejor manera de conseguirlo era bloqueando los canales de cloruro, así que enseguida pensó en la sustancia que podría ayudarle, la clorotoxina.
La sorpresa vino cuando Ullrich inyectó la clorotoxina en el cerebro de varios ratones con glioma. Por algún extraño motivo, la molécula se pegaba a las células tumorales y dejaba en paz a las células sanas. Aquello podía ser una vía muy interesante de investigación y junto al director de su laboratorio, Harald Sontheimer, no tardaron en encontrar una forma de utilizarlo: añadir alguna sustancia tóxica a la molécula que llegara únicamente a las células tumorales y acabara con ellas.
En aquellas fechas el doctor Jim Olson estaba empezando su carrera como oncólogo pediatra y trataba a un pequeño de 6 años llamado Hayden Strum. El niño sufría un glioma y después de muchas operaciones y sesiones de quimioterapia, Olson vio como las funciones neurológicas del chaval se deterioraban sin que pudieran hacer nada para impedir su muerte. Aquella experiencia, recuerda Olson, fue como un aldabonazo en su conciencia y tomó la decisión de dedicar todos sus recursos y esfuerzos a encontrar la manera de que nadie tuviera que pasar por algo similar.
Uno de los problemas que atormentaba a Olson, y a todos los cirujanos que se enfrentan a un tumor cerebral, era el dilema que se plantea a la hora de eliminar los tejidos tumorales. Si el médico retira demasiado poco tejido corre el riesgo de no eliminar el tumor totalmente y se reproduzca a partir de los bordes. Si retira demasiado, hay algunas zonas puede provocar efectos secundarios en el paciente. Y la cuestión es aún más terrible cuando se trata de niños.
En la búsqueda de una solución a este problema, Olson se encontró con los trabajos de Ullrich y su equipo y empezó su propia línea de investigación. La clorotoxina de Sontheimer ya estaba en fase de ensayos clínicos y Olson tuvo que pagar 100.000 dólares para acceder la molécula. Pero pronto empezaron a obtener sus propios resultados y vieron que el péptido se pegaba a las células tumorales de cualquier tipo de cáncer - desde los de piel a los de pulmón - y que la molécula pasaba sin problemas la barrera hematoencefálica, lo que permitía administrarla por vía intravenosa y no localmente en el cerebro del paciente.
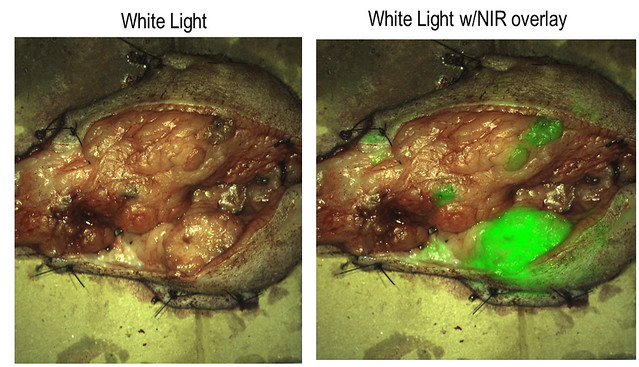 Localización de un tumor mamario en un perro. Los puntos secundarios iluminados a la derecha pasarían desapercibidos en una operación normal (Imagen: Blaze Bioscience)
Localización de un tumor mamario en un perro. Los puntos secundarios iluminados a la derecha pasarían desapercibidos en una operación normal (Imagen: Blaze Bioscience)La siguiente idea fue utilizar la clorotoxina como vehículo de transporte no de sustancias que acabaran con el tumor, sino de marcadores luminosos. En este caso añadieron una molécula que emite luz en el infrarrojo llamada Cy5.5. y probaron a inyectar la mezcla de clorotoxina y moléculas fluorescentes en los tumores de un ratón. En menos de una hora, las células cancerígenas del cerebro del ratón estaban brillando y señalando su posición con una sensibilidad 500 veces mayor que las de la resonancia magnética funcional. El sistema, que presentaron en la prestigiosa revista Cancer Research y patentaron como Tumor Paint, era capaz de iluminar las células tumorales más pequeñas y de marcar el camino del cirujano a la hora de operar.
"Los escorpiones han evolucionado durante millones de años, han desarrollado una proteína que llega hasta el cerebro de sus presas y las paraliza", explica Olson, que trabaja para el Centro Fred Hutchinson del Cáncer y el Hospital Infantil de Seattle. "Resulta que estas pequeñas proteínas en su veneno se pegan a las células cancerosas y no a las tejidos normales por motivos que aún no entendemos. Lo que hicimos fue acoplar unas moléculas fluorescentes a esto y cuando entran en el torrente sanguíneo nos indican dónde está el tumor".
El camino de Olson, plagado de trabas y de investigadores que le decían que era demasiado optimista, está a punto de llegar al punto culminante. Hace tan solo unos días, la FDA (autoridad que regula los medicamentos en EEUU) ha dado su aprobación para que comience la Fase I del ensayo clínico en humanos, que se llevará a cabo conjuntamente en Estados Unidos y Australia. Este primer estudio se centrará en 21 pacientes con glioma con los que se probará el producto Tumor Paint BLZ-100, que se inyecta en los tejidos y permite distinguir las células tumorales durante la operación. La compañía de Olson (Blaze Bioscience) considera que si los resultados son exitoso podrían lanzar su clorotoxina luminosa al mercado en un plazo de 5 años, donde competirán con otros sistemas de señalización de tumores como el ácido Aminolevulínico (5-ALA) una molécula que también se pega a los gliomas y los señaliza en color rojo y que ya se está utilizando en los quirófanos.
Aparte de mejorar el tratamiento de los tumores cerebrales en niños, la parte más interesante del proyecto de Olson es que aseguran haber encontrado una manera mucho más rápida de analizar el genoma de distintos organismos vivos en busca de estos péptidos (a los que llaman óptidos) que la naturaleza ha perfeccionado durante miles de años en el ‘horno’ de la evolución. "En 2011 obtuvimos 12 candidatos a óptidos en un año”, aseguran, "¡Ahora podemos obtener 10.000 en tres semanas!". La idea de Olson, bautizada como proyecto Violeta, es obtener muchos candidatos para encontrar sustancias que ayuden a combatir enfermedades que hasta ahora han tenido poca atención, como los centenares de enfermedades raras para las que aún no hay un tratamiento. Y si el análisis masivo de estas sustancias tiene éxito, tal vez algún día la humanidad contraiga una deuda impagable con el veneno de escorpión.
Más info: Proyecto Violeta | How Nature and a 9-Year Old Are Revolutionizing Cancer Treatmen (TEDxSeattle) | One Doctor’s Quest to Save People by Injecting Them With Scorpion Venom (Wired) | Tumor Paint: Changing the way surgeons fight cancer (CNN) | Trabajos publicados
* Este artículo es una colaboración el blog de biotecnología Biotekis coordinado por mi amigo Óscar Menéndez. No dejéis de visitarlo.















